Wako的LAL系统对内毒素检测技术的贡献-获得FDA认可

内毒素是革兰氏阴性菌细胞壁成分中的一种强效毒素。一旦进入到人的血液中,就会引起发热或致死性休克,因此,我们必须保证药物没有受到内毒素的污染。FUJIFILM Wako研发生产裂解试剂(鲎试剂)和检测仪器“Toxinometer”,不断推动内毒素检测技术的进步,30多年来一直支持药物的发展。
◆从裂解试剂的进口销售到内毒素检测仪器的开发

FUJIFILM Wako位于美国的工厂(地址:弗吉尼亚州里士满)
最初,内毒素检测采用的是兔热源试验。将试剂注射到兔子体内,再根据兔子体温的上升程度判断内毒素的含量。但该试验耗时长,而且使用动物的方法无法保证可靠的结果。
1956年,美国动物学家F.B.Bang发现鲎的血液能使内毒素凝固,他利用鲎的血细胞提取物配制出内毒素检测试剂(鲎试剂,后改名为裂解试剂),随后又利用该试剂开发出了“凝胶法”。凝胶法在1980年被收录到美国药典中,而在此之前FUJIFILM Wako就已经开始进口和销售内毒素检测试剂。但凝胶法只是一种半定量法,其精确度会受检测者操作熟练度的影响。
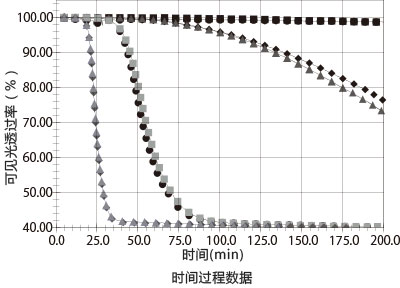
为解决上述问题,FUJIFILM Wako在1985年通过对传统原理的改进,首次开发出“浊度-时间分析法”和检测仪器“Toxinometer-ET-201”。与此同时,美国ACC公司(Associates of Cape Cod,.INC)利用相同的检测原理,开发出“LAL-5000”检测系统。基于这一情况,浊度-时间分析法在1987年被收录在美国食品药品监督管理局指南中。
FUJIFILM Wako的技术开发仍在继续,1988年开发出面向少量样品用户的“Toxinometer-ET-208”,1994年升级的第二代“Toxinometer-ET-301”集收集检测数据和数据处理、报告输出等功能于一体,深受广大制药商的欢迎。
在2004年发售了第三代“ET-5000”后,目前,FUJIFILM Wako提供支持浊度法、显色法、凝胶法“Toxinometer-ET-7000”和多种试剂。作为内毒素检测的先驱,FUJIFILM Wako一直对药物的安全生产和品质管理做出贡献。
◆竭力推广内毒素检测技术
目前,药典中记录的3种内毒素检测法分别为凝胶法、浊度法和显色法。除此之外还有药典未收录的β-葡聚糖检测、肽聚糖检测(SLP试剂)等多种试验法,每种试验法在操作时都有需要注意的地方。
例如,在内毒素检测试验中需要关注试验用具、试验用水等细节。在以药典为基础的试验中则规定进行预试验和定量检测。内毒素的添加方法和求最大有效稀释率对于新手而言可能会有些困难。另一方面,试剂也有多种变化。需要根据试剂的水溶性或不同的动物血液和培养基适当调整检测方法。虽然FUJIFILM Wako会提供“内毒素试验法”手册,但其他手册中未涵括的试验法则需要在操作中多加注意。
凭借1996年日本药典第13次改版中新收录了浊度法和显色法的契机,FUJIFILM Wako首创开展研讨会。此后,每年开展的研讨会都致力传播内毒素检测相关信息、药典中更正的注意事项以及国际动向等信息。自2008年以来,FUJIFILM Wako开始举行内毒素试验法技术研讨会,专注于实验技术的传播。
◆设立获FDA认可的工厂,开发世界唯一的内毒素特异性试剂
世界上第一瓶裂解试剂是在美国开发的,而最初FUJIFILM Wako销售的裂解试剂也是从美国进口的产品。
随着“Toxinometer”的面世,市场开始扩大,试剂需求逐步提高,FUJIFILM Wako在美国建立起了自己的工厂。除了因为当地有丰富的原料鲎以外,还能通过获得以监管严格著称的FDA认可来保证产品的质量。生产出来的试剂必须获得FDA的认可才能在美国及海外销售。
2003年,FUJIFILM Wako收购了位于圣路易斯的Hemakem公司作为进入美国市场的立足点。然后在里士满建立新工厂,获得FDA认可并开始生产试剂。而且FUJIFILM Wako的产品是世界上唯一获得FDA认可的内毒素特异试剂。
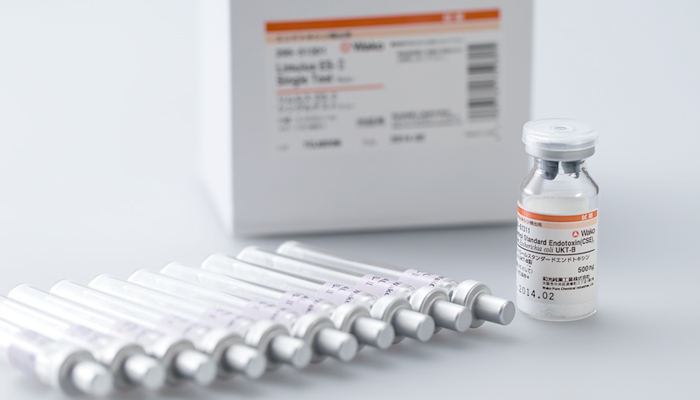
试剂会在试管内预先冻干,还有只需添加试剂即可进行检测的单一型试剂盒。在该领域中,世界上也是只有FUJIFILM Wako的内毒素特异试剂获得了FDA的认可。
30年来,FUJIFILM Wako一直参与检测法的改进与“Toxinometer”的开发,并作为日本内毒素检测先驱的一员,竭力推进药物行业的发展。
更多产品详情请点击:Wako的内毒素检测系统