USP拟新增 “使用重组鲎试剂进行细菌内毒素检测” 章节
![]()
2023年8月,USP微生物学专家委员会提出新增<86> Bacterial Endotoxins Test Using Recombinant Reagents(使用重组试剂进行细菌内毒素检测)章节的提议,并以General Announcement形式发布。该章节正式发布前,会在2023年11月1日至2024年1月31日期间征询意见。

“<86> Bacterial Endotoxins Test Using Recombinant Reagents will be published in Pharmacopeial Forum 49(6) [Nov.–Dec. 2023]. This proposal will include methods for recombinant Factor C (rFC) and recombinant cascade reagents (rCR) “
新提议的USP <86>中,将包含C因子重组鲎试剂法(rFC)以及重组级联鲎试剂法(rCR)这两种检测方法。
其中,重组级联鲎试剂法(rCR)的特点如下:
● 重组技术制备,不依赖天然鲎资源,可持续供应
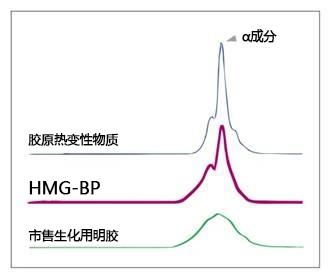
● 级联机制包含C因子、B因子和凝固酶原,与传统天然鲎试剂检测的相关性更高
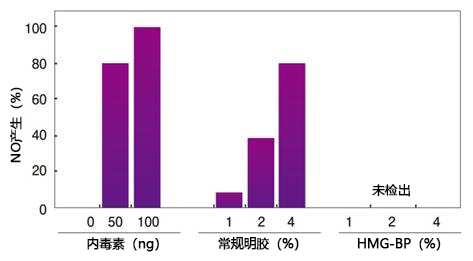
● 特异性检测,消除天然鲎试剂中因G因子而导致的(1→3)-β-D-葡聚糖假阳性反应
● 使用动力学法酶标仪即可检测,无需使用荧光酶标仪
针对重组级联鲎试剂法(rCR),FUJIFILM Wako可提供重组级联鲎试剂PYROSTAR™ Neo (点击图片了解更多)
此外,在Kikuchi等人的研究中[1],使用天然鲎试剂与PYROSTAR™ Neo等重组鲎试剂对六种自来水进行细菌内毒素检测。在该实验中,使用rFC和rCR重组鲎试剂进行的自来水内毒素检测,检测结果与天然来源的鲎试剂相似。
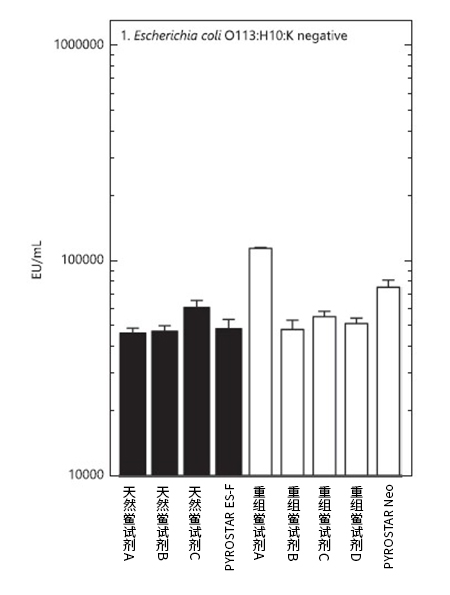
这意味着对于部分样品,或可考虑使用重组鲎试剂替代天然鲎试剂进行测试。
重组鲎试剂也有望应用于更多不同样品的检测。
点击此处查看相关产品详情:内毒素检测重组鲎试剂 PYROSTAR™ Neo
参考文献
[1] KIKUCHI, Y., MUROI, M., NAKAGAWA, Y., EBISAWA, A., HAYASHI, M., TAKEUCHI, H., … & TSUCHIYA, M. (2023). Collaborative Study of Bacterial Endotoxins Test Using Recombinant Factor C-Based Procedure for Detection of Lipopolysaccharides (Part 3). Pharmaceutical and Medical Device Regulatory Science, 54(4), 341-351.