人类多能干细胞(hPSCs)包括人类胚胎干细胞(hESCs)和人类诱导多能干细胞(hiPSCs)。这类干细胞具有无限的自我复制和多项分化潜能,是再生医学、疾病建模和药物筛选研究的重要工具。近年来,研究人员已开发出多种方案,通过导入外源基因或者利用小分子诱导等方法,将人类多能干细胞分化为骨骼肌细胞(SkMCs),从而为骨骼肌损伤和肌营养不良等肌肉相关疾病的研究和药物筛选提供了新的途径。虽然目前有许多方法可以将hPSCs分化成SkMCs,但大多数方法都涉及到3D球状胚体的形成以及细胞分选,过程复杂,难以大量获得肌原细胞,骨骼肌形成率极低,很大程度上影响了肌肉再生医学研究的进展。如能在“hPSCs分化为骨骼肌”研究方面取得突破,就能为细胞疗法或药物筛选带来充足的肌细胞,例如从肌营养不良患者体内取出的干细胞分化产生的肌原细胞,可为该患者的提供很好的治疗原料,同时还能对这类肌肉相关性疾病进行更深入的研究。因此,如何构建一个高效的体外肌原性祖细胞分化平台是突破肌肉再生医学研究领域的一个关键技术瓶颈。
这里小编为大家推荐一种非常简单但高效,仅需三个步骤就能将hPSCs分化为成熟骨骼肌细胞的新方法——来自Myocea公司的Skeletal Muscle Differentiation Kit(hPSC诱导分化骨骼肌试剂盒)。该方法的优点是仅需要单层细胞培养就可以制备出大量的SkMCs,而无需表达肌原性转录因子或细胞分选等额外操作。由于成肌祖细胞和成肌细胞具有很高的增殖能力,可以通过常规传代方式进行大规模扩增,从而获得大量分化的肌管细胞。因此,该方法非常简单高效,并且适用于自动化和大规模生产。实验表明,仅用6×104个hPSCs就可以生产出7.5×107个SkMCs,说明了该方法具有很高的效率和可扩展性。
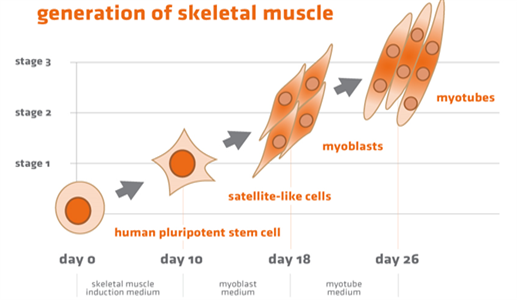
Myocea的Skeletal Muscle Differentiation Kit是世界首款能将hPSCs分化为骨骼肌细胞的商品化培养基系统,由四个培养基组成。通常情况下,从人多能干细胞生成肌细胞需要3个阶段(如上图),即依次生成卫星样祖细胞(satelite-like progenitor cells)和成肌细胞(myoblasts),最后融合成为多核肌管细胞(multinucleated myotubes)。因此Skeletal Muscle Differentiation Kit包含了三个分化阶段所需的三种培养基,此外它还提供了一个促进肌管融合的培养基作为可选组分,可根据研究者希望得到的细胞表型灵活选择。骨骼肌分化系统的四个培养基详情见下表。
|
货号 |
品名 |
|
SKM01-250mL |
Skeletal Muscle Induction Medium (Stage I) |
|
SKM02-250mL |
Skeletal Myoblast Medium (Stage II) |
|
SKM03-250mL |
Myotube Medium (Stage III, Option 1) |
|
SKM03+-250mL |
Myotube Fusion Medium (Stage III, Option 2) |
用该培养系统分化生成的肌细胞通常由70-90%的肌管细胞和10-25%的肌前体细胞组成。如下图细胞标志物染色显示肌细胞表型成熟且功能完整。
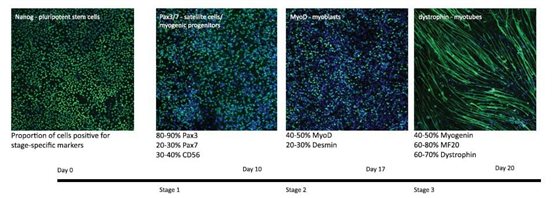
更重要的一点是,通过标志物的核酸与蛋白表达水平的比对发现,该方法具有很高的可重复性,几株不同的干细胞系分化实验比对显示组间差异很小,稳定性非常好。因此,Skeletal Muscle Differentiation Kit还适用于高通量筛选和药物开发。
综上所述,Skeletal Muscle Differentiation Kit包括了以下优势特点,确实是一个令人心动的骨骼肌分化方案。
- 肌细胞生成率高。
- 三步法操作简单,无需细胞分选,无需表达肌原性转录因子。
- 实现了成肌细胞的扩增和储存,从而建立可再生的肌细胞库。
- 方法稳定,重复性好。

Myocea, Inc.是一家专注于提供神经肌肉疾病领域产品与服务的公司,是能够为相关制药企业提供专业试剂与合同服务的学术型战略合作者。Myocea公司是目前世界上拥有较大的人类胚胎干细胞的细胞库之一,并已开发和推出了世界首款稳定、高效且可扩展的专业骨骼肌细胞分化培养基系统。
上海金畔生物科技有限公司是Myocea品牌的中国区一级代理商,为用户提供完善的技术支持与售后服务。如对以上产品感兴趣,欢迎拨打上海金畔生物科技有限公司客服热线021-50837765或登录网站www.jinpanbio.cn了解更多信息。
参考文献:
A Human Pluripotent Stem Cell Model of Facioscapulohumeral Muscular Dystrophy-Affected Skeletal Muscles. Stem Cells Transl Med. 2016 Sep;5(9):1145-61.
